Çözeltiler: Temel Kavramlar ve Uygulamalar
Çözelti Nedir?
Çözelti, iki veya daha fazla maddenin homojen karışımıdır. Bir çözeltide:
- Çözücü (solvent): Genellikle miktarı fazla olan bileşen (örn: su)
- Çözünen (solute): Genellikle miktarı az olan bileşen (örn: tuz)
Günlük Hayattan Örnekler
- Tuzlu su (NaCl + H₂O)
- Şekerli çay (Şeker + Su + Çay bileşenleri)
- Hava (N₂ + O₂ + diğer gazlar)
Çözelti Hazırlama Yöntemleri
1. Katı-Sıvı Çözeltileri
Örnek: 0.1 M NaCl çözeltisi hazırlama:
- 5.844 g NaCl tartılır (1L için)
- 800 mL saf suda çözülür
- Hassas olarak 1 L'ye tamamlanır
2. Sıvı-Sıvı Çözeltileri
Örnek: %70'lik etanol çözeltisi:
- 700 mL saf etanol alınır
- 300 mL saf su eklenir
- Homojen olana kadar karıştırılır
UYARI: Etanol-su karışımlarında hacim daralması olur! 700 mL etanol + 300 mL su ≠ 1000 mL çözelti
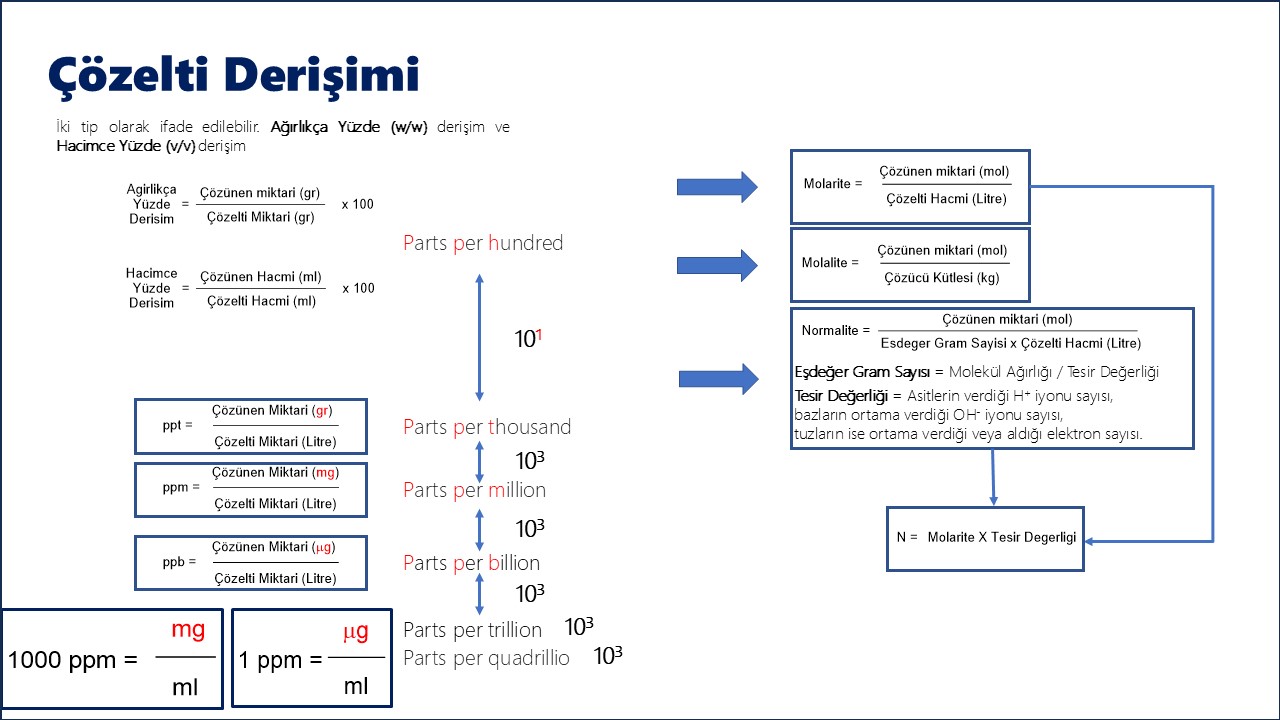
Derişim Birimleri
| Birim | Formül | Kullanım Alanı |
|---|---|---|
| Molarite (M) | mol çözünen / L çözelti | Laboratuvar çözeltileri |
| Molalite (m) | mol çözünen / kg çözücü | Sıcaklık değişimli deneyler |
| Kütlece % | (g çözünen / g çözelti) × 100 | Ticari ürünler |
| ppm (milyonda bir) | mg çözünen / kg çözelti | Çok seyreltik çözeltiler |
| ppb (milyarda bir) | μg çözünen / kg çözelti | Toksin analizleri |
Derişim Birimleri
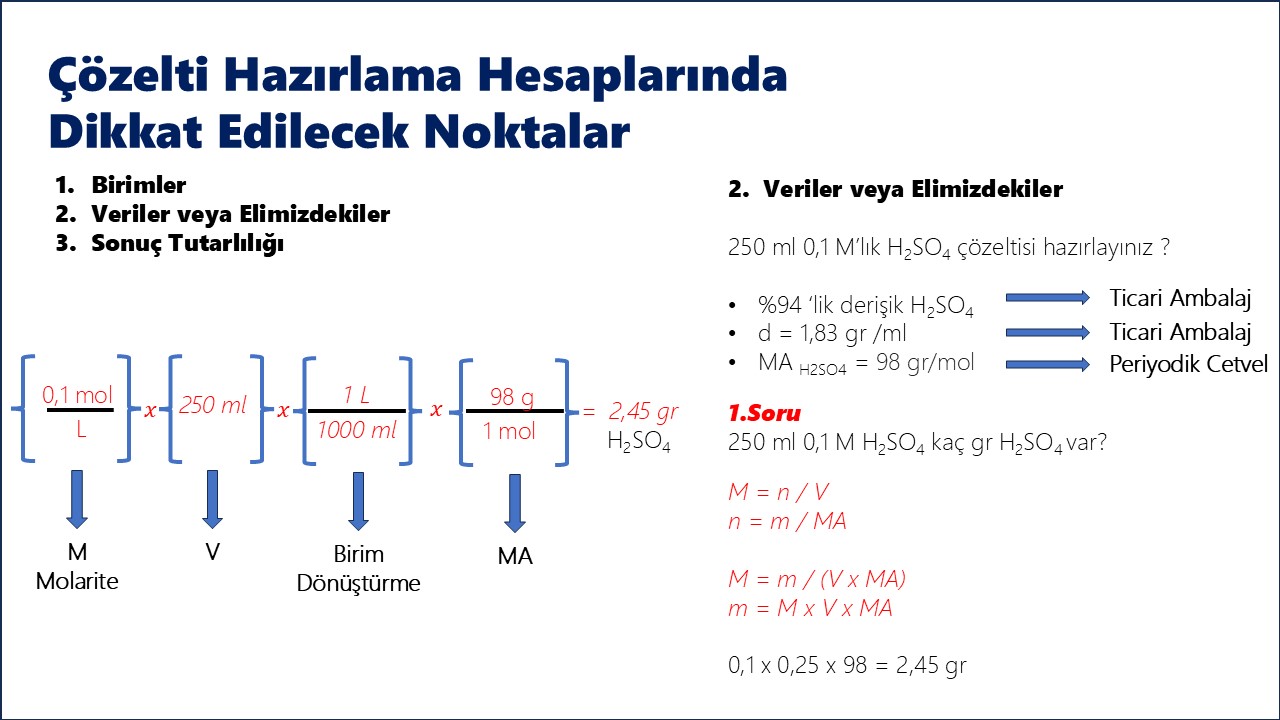
1. Molarite (M)
Formül: M = nçözünen / Vçözelti (L)
Birim: mol/L
Örnek: 500 mL'lik 0.2 M NaOH çözeltisi hazırlamak için kaç gram NaOH gereklidir? (NaOH: 40 g/mol)
2. Molalite (m)
Formül: m = nçözünen / mçözücü (kg)
Birim: mol/kg
Örnek: 250 g suda 2.5 g etilen glikol (C2H6O2) çözülerek hazırlanan çözeltinin molalitesi nedir? (C2H6O2: 62 g/mol)
3. Kütlece Yüzde (%w/w)
Formül: %(w/w) = (mçözünen / mçözelti) × 100
Birim: %
Örnek: 40 g şeker ve 160 g su karıştırılarak hazırlanan çözeltinin kütlece yüzdesi nedir?
4. Hacimce Yüzde (%v/v)
Formül: %(v/v) = (Vçözünen / Vçözelti) × 100
Birim: %
Örnek: 150 mL etanol ve 350 mL su karıştırılıyor. Etanolün hacimce yüzdesi nedir?
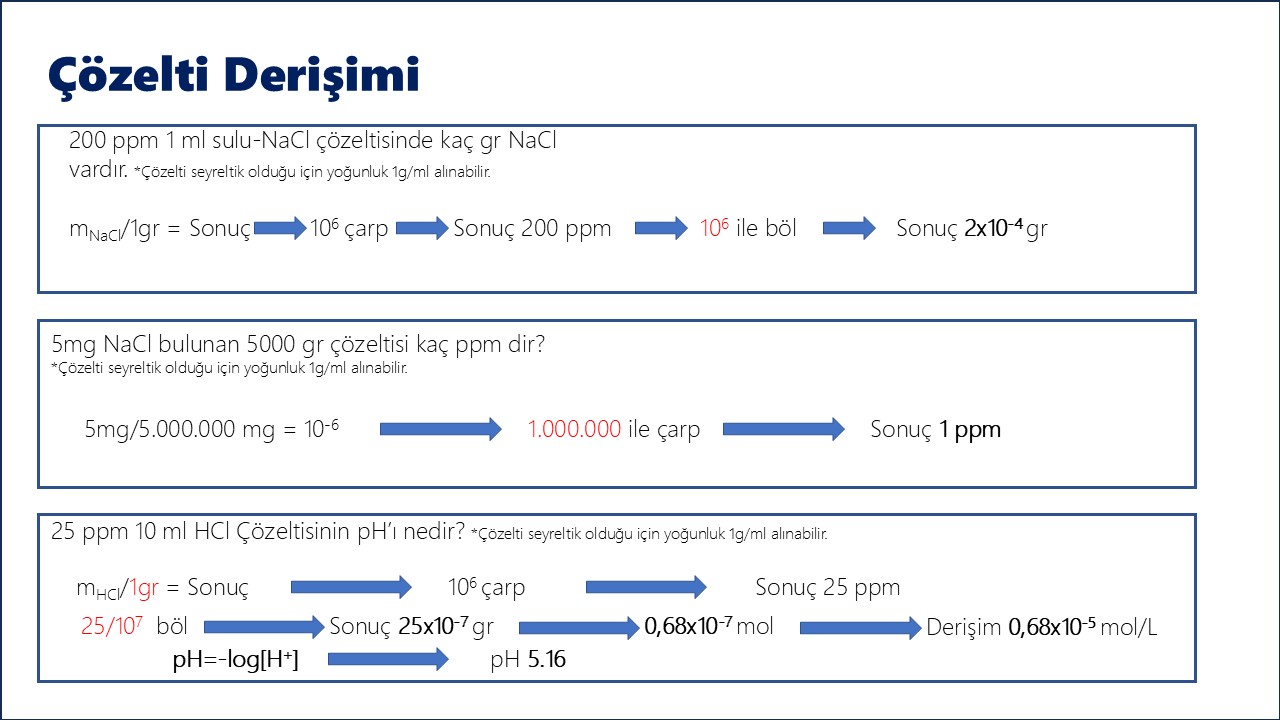
5. ppm (milyonda bir)
Formül: ppm = (mçözünen (mg) / mçözelti (kg))
Birim: mg/kg
Örnek: 2 kg çözeltide 8 mg kurşun iyonu varsa konsantrasyon kaç ppm'dir?
6. ppb (milyarda bir)
Formül: ppb = (mçözünen (μg) / mçözelti (kg))
Birim: μg/kg
Örnek: 500 g çözeltide 25 μg cıva varsa konsantrasyon kaç ppb'dir?
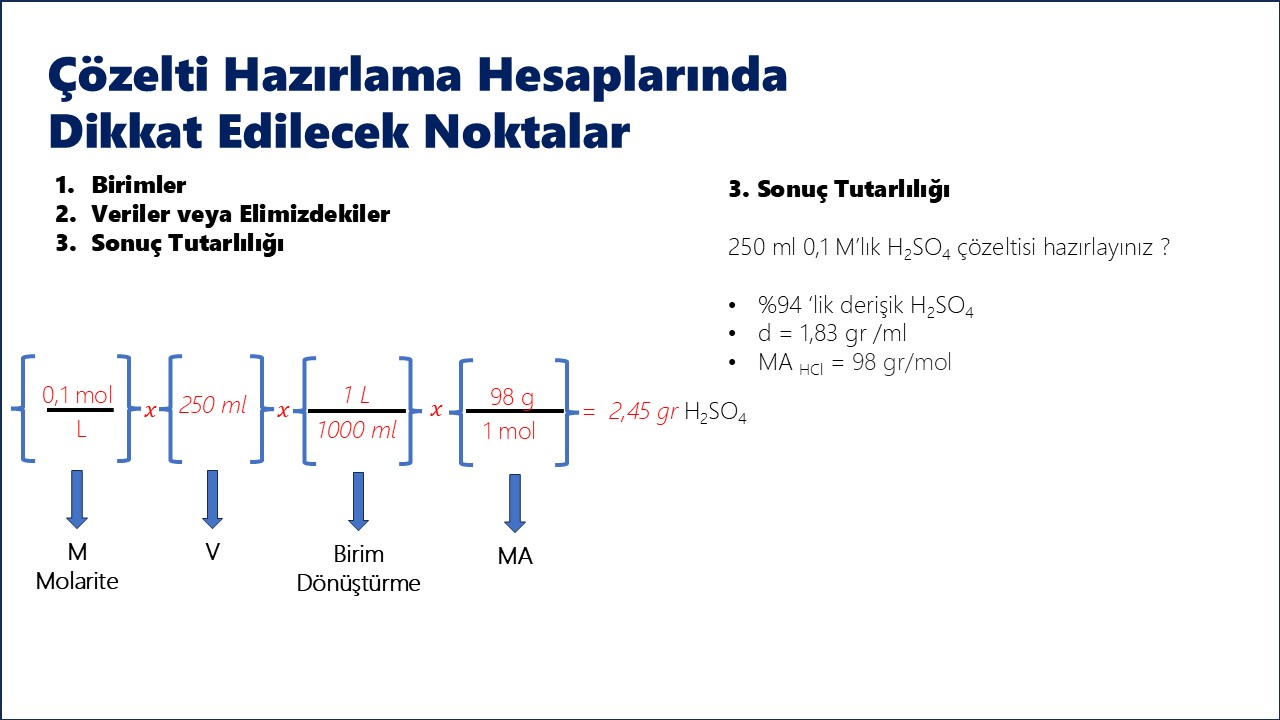
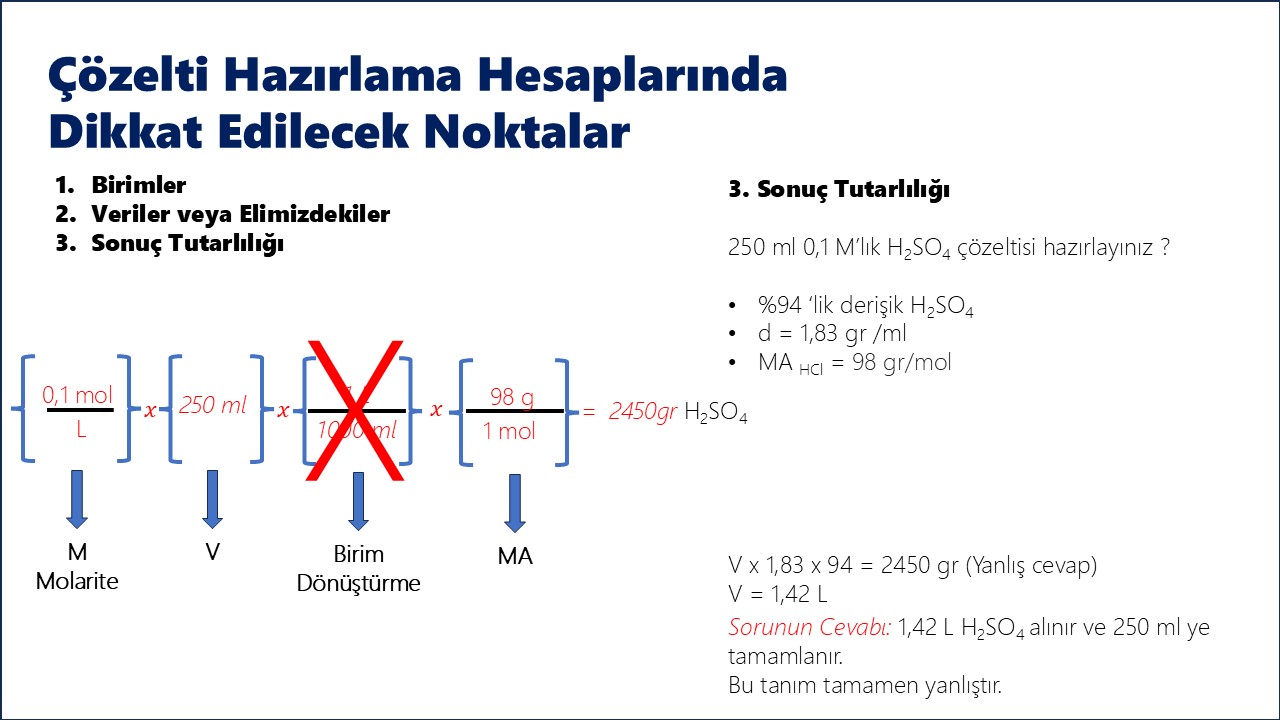
7. Normalite (N)
Formül: N = neşdeğer / Vçözelti (L)
Birim: eşdeğer/L
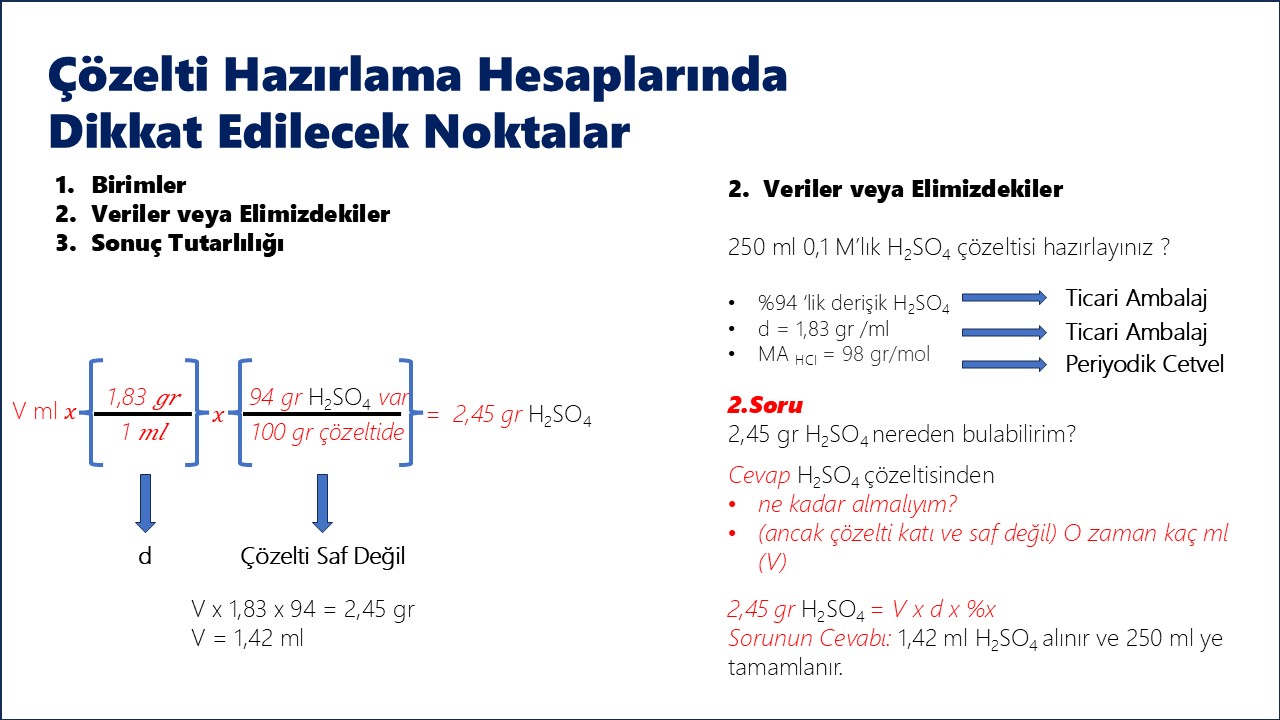
Örnek: 250 mL'lik 0.1 N H2SO4 çözeltisi hazırlamak için kaç gram asit gerekir? (H2SO4: 98 g/mol)
Örnek Hesaplama: Molarite
53 g Na₂CO₃ ile 500 mL çözelti hazırlanıyor. Molarite nedir? (Na₂CO₃: 106 g/mol)
Kristallendirme ve Çöktürme
Kristallendirme Adımları
- Doygun çözelti hazırlanır (sıcak çözücüde)
- Sıcakken süzülür (çözünmeyenler ayrılır)
- Yavaşça soğutulur
- Oluşan kristaller süzülerek ayrılır
- Uçucu olmayan çözücülerde yıkanır
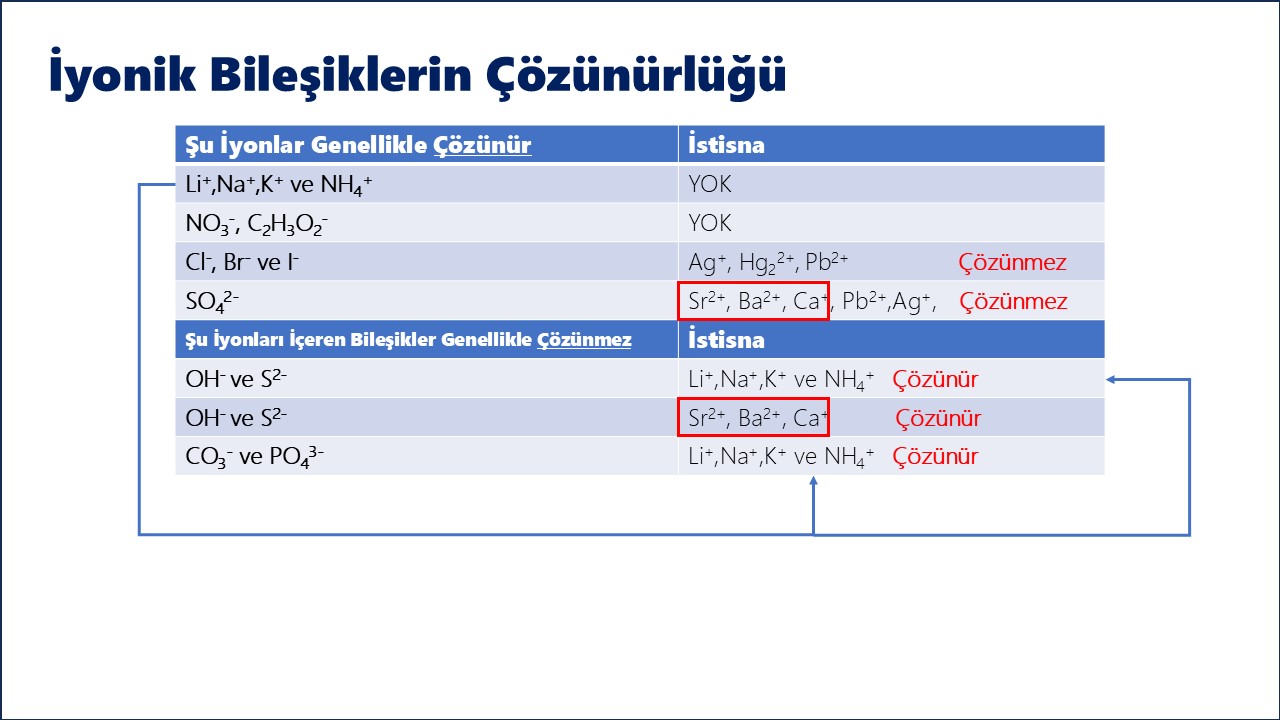
Çöktürme Yöntemleri
- Ortak iyon etkisi: Çözünürlüğü azaltan iyon eklemek
- pH ayarı: Özellikle metal hidroksitler için
- Sıcaklık değişimi: Çözünürlüğü sıcaklıkla azalan maddeler
Laboratuvar Uygulaması: Bakır Sülfat Kristallendirmesi
1. 100 mL kaynar suda 50 g CuSO₄ çözülür
2. Sıcakken süzülür
3. Oda sıcaklığında 24 saat bekletilir
4. Mavi kristaller süzülür, etanolle yıkanır
Çözünürlük ve Etkileyen Faktörler
| Faktör | Etkisi | Örnek |
|---|---|---|
| Sıcaklık | Genellikle katılarda artar, gazlarda azalır | Şekerin sıcak suda çözünmesi |
| Basınç | Gazlarda belirgin artış | CO₂'nin soda şişesinde çözünmesi |
| Çözücü türü | "Benzer benzeri çözer" kuralı | Yağın suda çözünmemesi |
Uygulama Soruları
Soru 1: 250 mL'sinde 4.9 g H₂SO₄ içeren çözeltinin molaritesi nedir? (H₂SO₄: 98 g/mol)
Soru 2: 500 g suda 2 mol NaCl çözülerek hazırlanan çözeltinin molalitesi nedir?
Önemli Uyarılar
- Hacimce karışımlarda (etanol-su gibi) toplam hacim korunmayabilir
- Molarite sıcaklığa bağlıdır (hacim değişir), molalite değildir
- Kristallendirme için yavaş soğutma daha büyük kristaller verir
- Çözelti hazırlarken daima çözücüyü son hacme kadar ekleyin